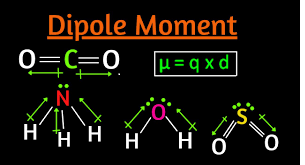
این اثر را اوّلین بار « دبای » (Debye) در رابطه با القای قطبیّت به وسیله مولکول قطبی در یک مولکول غیر قطبی کشف کرد . بیان می کند که : هر مولکول غیر قطبی و یا یون نامتقارن ( غیر قطبی ) که در یک میدان الکتریکی به شدّت E قرار گیرد ، قطبش در آن به وجود می آید یعنی این که مرکز بار های مثبت و منفی آن از هم جدا و دارای دو قطب مثبت ومنفی مجزّا از یکدیگر می شود . به عبارتی دیگر این ذرّه دارای یک ممان ( گشتاور ) دو قطبی الکتریکی می شود . که این امر باعث می شود که در راستای میدان جهت گیری کند .
را مُمان دو قطبی القایی آن ذرّه در میدان الکتریکی می نامند و بین آن و شدت میدان الکتریکی رابطه :
برقرار است .
نسبت به
را قطبیّت پذیری آن ذره می نامند . هر چه ذرّه غیر قطبی حجیم تر باشد ، تعداد الکترون های آن بیشتر است . بر همین اساس است که قطبیت پذیری هالوژن ها با افزایش عدد اتمی آنها بیشتر می شود . مثلا قطبیّت پذیری یُد یا آینون یُدید
از قطبش پذیری بُرم یا آنیون بُرمید
بیشتر است .
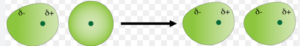
هر مولکول قطبی و یا هر کاتیون ، می تواند در نقش یک میدان الکتریکی مولکول های غیر قطبی یا آنیون ها راقطبی کند . بدیهی است هر چه مُمان دو قطبی مولکول قطبی بیشتر باشد ، قدرت قطبی کنندگی آن بیشتر است .در شکل مقابل ، طرحی از چگونگی قطبی شدن یک مولکول ناقطبی به وسیله یک مولکول قطبی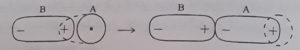
نشان داده می شود . در مورد کاتیون ها نیز هرچه کاتیون کوچک تر باشد ، چگالی بار الکتریکی آن بیشتر استّ یعنی پتانسیل یونی ( نسبت بار به شُعاع ) آن بزرگتر است و یا این که اگر بارموثّر هسته آن بزرگ تر باشد ، قدرت قطبی کردن آن بیشتر است . ( قاعده فاجانس ) آنیون نیز هرچه نرمتر باشد ، یعنی اندازه آن بزرگ و بار الکتریکی آن بیشتر باشد ، بهتر و بیشتر قطبیّت حاصل می کند .
در شکل مقابل چگونگی پُلاریزاسیون یک آنیون به وسیله یک کاتیون نشان داده شده است .
البته امکان قطبی شدن کاتیون به وسیله آنیون را هم در نظر داشته باشیم . اگر کاتیون دارای بار کم و حجم بیشتر باشد ،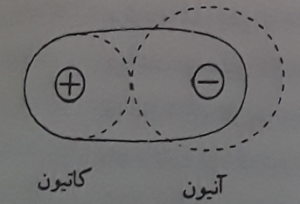
مثلاً آنیون هایی مثل و
در کمپلکس های مربّعی در حالت ترانس می تواند اتم مرکزی را که یک کاتیون فلز واسطه است ، قطبی کند .
اثر قطبیّت پذیری در ترکیب های یونی عامل پیدایش خصلت کووالانسی در آنها خواهد بود ، یعنی به علت همپوشانی ابرهای الکترونی کاتیون و آنیون قطبی شده ، تا حدّی پیوند کووالانسی نیز علاوه بر پیوند یونی
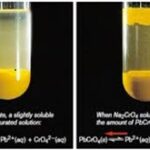
در شبکه بلور تشکیل می شود . این عمل باعث می شود که برخی از خواص ویژه در ترکیب یونی آشکار شود ، از جمله میزان انحلال پذیری آن در حلّل قطبی مانند آب کاسته می شود . علّت این که هالیدهای نقره با افزایش عدد اتمی هالوژن ، یعنی افزایش حجم آنیون هالید در آب ، از میزان انحلال پذیری آن در آب کاسته می شود همین اثر پُلاریزاسیون و قطبی شدن یون های هالید است . چون یون یُدید
از یون
بُرمید و این دو یون نیز بیشتر از یون کُلرید
به وسیله کاتیون نقره
قطبش حاصل می کنند ، از
تا
به تدریج خصلت کووالانسی افزایش می یابد و به موازات آن از میزان انحلال پذیری هالید نقره کاسته می شود . امّا چرا نقره فلوئورید
در آب به خوبی حل می شود ، علّت این است که یون فلوئورید
به وسیله یون نقره
پُلاریزه نمی شود و
خصلت یونی به نسبت کاملی دارد و در نتیجه در آب که یک حلّال قطبی است به خوبی حل می شود .
- دبای ، شیمی فیزیکدان آمریکایی که نخستین کار علمی او ، توجیه نظری گشتاورهای دو قطبی بود .